Hoffmann, M., Pöhlmann, S. Nuevos receptores del SARS-CoV-2: ASGR1 y KREMEN1. Cell Res (2021). https://doi.org/10.1038/s41422-021-00603-9
Recopilado por Carlos Cabrera Lozada. Miembro Correspondiente Nacional, ANM puesto 16. ORCID: 0000-0002-3133-5183. 24/12/2021
Se cree que la interacción de la proteína espiga del SARS-CoV-2 con el receptor celular ACE2 es esencial para la entrada viral en las células huésped. En un artículo reciente publicado en Cell Research,Gu y sus colegas informan que ASGR1 y KREMEN1 también pueden servir como receptores de SARS-CoV-2 y podrían afectar el rango de células diana virales y la neutralización mediada por anticuerpos.
La proteína espiga (S) del coronavirus facilita la entrada viral en las células. Para ello, la proteína S activa los receptores celulares y el patrón de expresión y la secuencia de estos receptores determinan principalmente qué células y especies pueden infectarse. Un dominio de unión al receptor (RBD), ubicado en la unidad de superficie, S1, de la proteína S, interactúa con los receptores. Los RBD en las proteínas S del SARS-CoV y el SARS-CoV-2, los agentes causantes del SARS y el COVID-19, respectivamente, exhiben homología de secuencia y se unen a la enzima convertidora de angiotensina 2 (ACE2) para la entrada de la célula huésped.1,2
Para causar enfermedad en ratones, se requiere la adaptación del SARS-CoV y el SARS-CoV-2 a la ACE2 murina o la expresión dirigida de ACE2 humana en tejidos murinos y la eliminación de ACE2 reduce fuertemente la propagación viral.3 Además, la susceptibilidad de las líneas celulares a las infecciones por SARS-CoV y SARS-CoV-2 se correlaciona en gran medida con la expresión de ACE2. Sin embargo, esta correlación no es absoluta y un estudio reciente informó de la entrada de SARS-CoV-2 independiente de ACE2 en una línea celular pulmonar.4 Además, el SARS-CoV-2,5 como el SARS-CoV,6 puede infectar un amplio espectro de células, tejidos y órganos en pacientes humanos y se ha documentado evidencia de infección por SARS-CoV-2 de células que expresan niveles bajos o ningún ACE2. Sin embargo, los factores celulares que apoyan la entrada independiente de ACE2 han permanecido en gran medida esquivos.
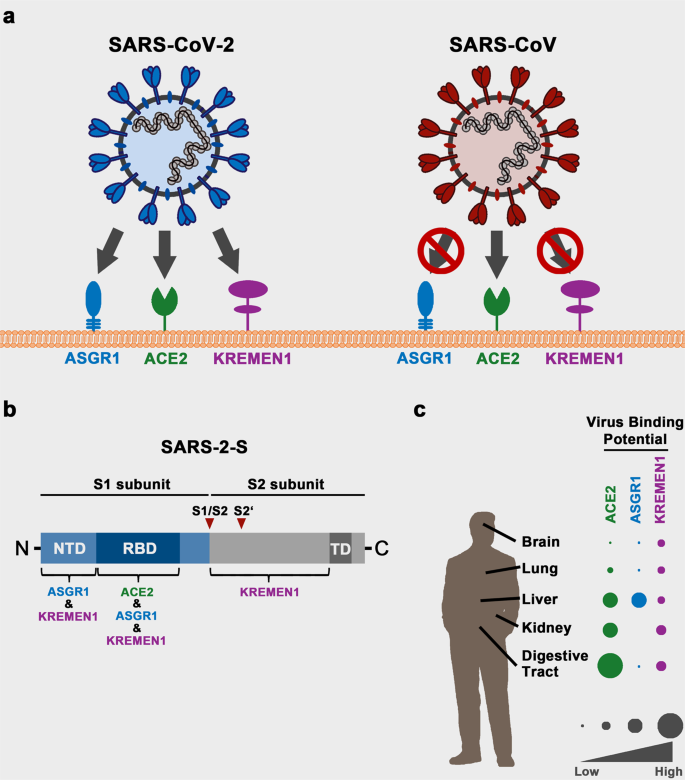
En un artículo reciente de Investigación Celular, Gu y sus colegas identificaron las proteínas celulares asialoglycoprotein receptor-1 (ASGR1) y Kringle Containing Transmembrane Protein 1 (KREMEN1) como socios de unión a la proteína S.7 Expresión dirigida de ASGR1 y KREMEN1 en un ACE2– línea celular permitida para la entrada de SARS-CoV-2 pero no de SARS-CoV (Fig. 1a). Se obtuvieron resultados similares para la infección por SARS-CoV-2 en un modelo de ratón, aunque la entrada a través de ASGR1 y KREMEM1 fue generalmente menos eficiente en comparación con la entrada dependiente de ACE2.
Los estudios de inhibición y derribo de anticuerpos revelaron que KREMEN1 endógeno o ASGR1 era, junto con ACE2, necesario para la entrada del SARS-CoV-2 en ciertas líneas celulares. La entrada en una línea celular derivada de pulmón, HTB-182, y una línea celular derivada del hígado, Li7, fue independiente de ACE2 y KREMEN1- (células HTB-182) o asgr1-dependiente (células Li7), y se asoció con resistencia a anticuerpos neutralizantes dirigidos a la interfaz proteína S/ACE2. Por lo tanto, ASGR1 y KREMEN1 son receptores de buena fe del SARS-CoV-2 que podrían proteger al virus de ciertos anticuerpos neutralizantes.
El análisis de muestras clínicas reveló que la expresión relativa de ACE2, ASGR1 y KREMEN1 en el epitelio respiratorio fue mayor en las células infectadas por SARS-CoV-2 en comparación con las células no infectadas. Además, la expresión de KREMEM1 en células secretoras se correlacionó más fuertemente con la susceptibilidad a la infección que la expresión de ACE2. Los anticuerpos específicos de ASGR1 y KREMEN1 bloquearon la unión a la proteína S y la entrada en las líneas celulares y redujeron la infección de los organoides pulmonares, lo que sugiere un papel de estos factores en la infección por SARS-CoV-2 del tracto respiratorio.
Se ha informado que varios factores celulares distintos de ACE2 promueven la entrada de SARS-CoV y / o SARS-CoV-2, incluidos los proteoglicanos de sulfato de heparán8 y glicolípidos que contienen ácido siálico.9 Sin embargo, ASGR1 y KREMEN1 se destacan porque cumplen con el criterio central para un receptor: su expresión hace que las células sean susceptibles a la infección que de otro modo no serían susceptibles. Esto plantea varias preguntas interesantes:
¿Cuáles son las «mecánicas» de la entrada mediada por ASGR1 y KREMEN1? Se ha propuesto que la unión a ACE2 induce cambios conformacionales sutiles en la proteína S que promueven la activación proteolítica. Parece poco probable que ASGR1 y KREMEN1 induzcan cambios similares y la activación de la proteína S durante la entrada dependiente de ASGR1 / KREMEN1 aún no se haya examinado. Un enfoque de estos estudios debe estar en tmPRSS2 vs dependencia de catepsina L y el papel de los factores de restricción IFITM2/3.
¿Cómo se involucra el SARS-CoV-2 S (SARS-2-S) en ASGR1 y KREMEN1 y por qué el SARS-CoV S (SARS-S) no lo hace? Gu y sus colaboradores muestran que no solo el RBD sino también el dominio N-terminal (NTD) del SARS-2-S se unen a ASGR1 y KREMEN1 (Fig. 1b). Por lo tanto, las diferencias pronunciadas entre las secuencias NTD sars-S y SARS-2-S podrían, al menos en parte, explicar el fracaso del SARS-CoV para activar ASGR1 y KREMEN1 para la entrada.
¿Por qué la entrada dependiente de ASGR1 o KREMEN1 se asocia con resistencia contra la neutralización por anticuerpos? Una vez más, la unión del SARS-2-S NTD a ASGR1 y KREMEN1 podría tener la respuesta, ya que estas interacciones no deben ser inhibidas por el anticuerpo 404 específico de RBD, uno de los dos anticuerpos analizados por Gu et al. El segundo anticuerpo, 515, no se une a la RBD, pero podría dirigirse a una superficie de proteína S que puede modular ace2 pero no la unión a ASGR1/KREMEN1. Los experimentos con anticuerpos adicionales y ACE2 soluble deben proporcionar claridad. Puray-Chavez et al. y Ramírez y sus colegas informaron que la entrada independiente de ACE2 no se asoció con la resistencia a la neutralización.4,10 y las razones de estos resultados discrepantes aún no se han determinado.
¿El uso de ASGR1 y KREMEN1 difiere entre las variantes del SARS-CoV-2? El virus utilizado por Gu y sus compañeros de trabajo ha estado circulando al principio de la pandemia. Por lo tanto, se debe investigar si las variantes virales que surgieron más tarde y albergan mutaciones en la proteína S utilizan ASGR1 y / o KREMEN1 de manera más eficiente y si esto contribuye a la propagación viral. En particular, la entrada independiente de ACE2 hasta ahora solo se ha observado con proteínas S mutadas, con la mutación E484D desempeñando un papel importante.4,10
¿Qué tan prominente es la contribución de ASGR1 y KREMEN1 a la propagación del SARS-CoV-2 en humanos? Los análisis in silico predijeron que ACE2, ASGR1 y KREMEN1 pueden contribuir a la unión viral a varios tejidos (Fig. 1c),y los análisis de ARN-seq de muestras del tracto respiratorio superior de pacientes con COVID-19 proporcionaron evidencia de infección de ACE2–/KREMEN1 epitelial y ACE2+–/ASGR1 células inmunitarias. Sin embargo, no está claro si la absorción de partículas sin infección productiva fue responsable de algunas de las señales. Aunque ASGR1 y KREMEN1 contribuyeron a la infección de organoides pulmonares, ACE2 fue más importante. Por lo tanto, se requiere una mayor experimentación para aclarar esta cuestión.+
En resumen, la identificación de ASGR1 y KREMEN1 como receptores del SARS-CoV-2 avanza nuestra comprensión del tropismo celular y la patogénesis del SARS-CoV-2. Además, este hallazgo demuestra un impacto previamente no apreciado del tipo de célula objetivo en la neutralización mediada por anticuerpos.