https://doi.org/10.47449/CM.2020.1.1.27
Rafael Rangel-Aldao, Editor

Resumen Ejecutivo
Noticia de última hora: Moderna, Inc. anunció esta mañana que, «…el estudio de fase 3 de mRNA-1273, de su vacuna candidata contra COVID-19, reportó a Moderna que el ensayo cumplió con todos los criterios estadísticos pre-especificados en el protocolo, con una eficacia de la vacuna del 94,5%.» De igual forma, informaron que, «el criterio de valoración principal del estudio de fase 3 COVE se basó en el análisis de los casos de COVID-19 confirmados y adjudicados a partir de dos semanas después de la segunda dosis de vacuna. Este primer análisis intermedio se basó en 95 casos, de los cuales se observaron 90 casos de COVID-19 en el grupo de placebo versus 5 casos observados en el grupo de ARNm-1273, lo que resultó en una estimación puntual de la vacuna con una eficacia del 94,5% (p <0,0001).
El panorama desolador que muestra la figura de Johns Hopkins University, se podrá resolver al menos en parte, a partir de finales de año, con las dos candidatas a vacuna de esta semana, Pfizer y Moderna, ambas de tecnologías avanzadas y similares, a base del RNA mensajero de la espiga del virus. Varias lecciones se derivan de este hecho, 1) La aplicación exitosa y rápida de la ciencias básicas a la medicina traslacional y preventiva; 2) La fuente científica proviene de empresas de biotecnología, no de las grandes farmacéuticas ni de los gobiernos, pues Pfizer hizo un acuerdo con BionTech, y Moderna con el gobierno estadounidense; 3) Igual ocurrirá cuando se conozcan los resultados de la fase 3 de AstraZeneca y la Universidad de Oxford; 4) En apenas 11 meses desde la aparición del virus y la pandemia, de manera ultra acelerada se produjeron al menos dos candidatas a vacunas antivirales, de eficacia aparente mayor al 90%, lo que entre 2010 al 2020, tomó para otras vacunas, 8 años de desarrollo, 7 ensayos clínicos, 5.000 pacientes, y seis meses de seguimiento para su aprobación por la FDA. Otra lección de esta misma semana es que la contención y mitigación de la pandemia solo se puede lograr a través de la aplicación de la ciencia, como demuestra The Economist y el caso de Nueva Zelanda entre otros países, así como el de Uruguay en nuestro propio continente. El desarrollo de vacunas, no obstante, sigue lleno de grandes dudas e interrogantes, pues no conocemos la duración del efecto protector, ni tampoco las consecuencias inmunes de las mutaciones del virus y su transmisión de visones a humanos, por ejemplo, así como tampoco se termina de dibujar el panorama completo de la respuesta inmunológica multiorgánica al virus. En consecuencia, la vacunación podría ser efectiva en el control de la pandemia, pero estará sujeta a, «…las variaciones de la respuesta inmune a las infecciones primarias por SARS-CoV-2, y esa posible vacuna, podrá generar paisajes inmunes muy diferentes y cargas de casos críticamente graves, que van desde epidemias sostenidas hasta casi la eliminación de la pandemia». En Venezuela, la opción rusa no está repaldada por ensayos clínicos fiables, además que dispone de poca aceptación internacional, pues hay, fuertes críticas a la vacuna Gamaleya. Un mes antes del lanzamiento del ensayo de eficacia del Sputnik V en septiembre, la vacuna Gamaleya recibió una aprobación muy controvertida de las autoridades reguladoras rusas, que permitió que se administrara a personas fuera de un ensayo clínico.
Otro aspecto de las vacunas tiene que ver con la logística de distribución y administración de dos dosis por persona, que exige una cadena ultrafría como la de Pfizer, por ejemplo, que parece tener una desventaja ante Moderna, que soporta mayores temperaturas de conservación; en fin cómo diseñar una logística adecuada que permita pasar de los 30.000 a 50.000 vacunados de una fase 3, a los centenares de millones de humanos que en apenas pocos meses deberán ser vacunados entre 2021-2022. No hablemos de los aspectos demográficos de las vacunas, los grupos más vulnerables y poco representados en los ensayos de fase 3, niños y adultos mayores y de la gente y países de menores recursos económicos y sanitarios. Pero es indudable que hay progreso, mucho progreso científico, tecnológico y social hacia el control de la pandemia.
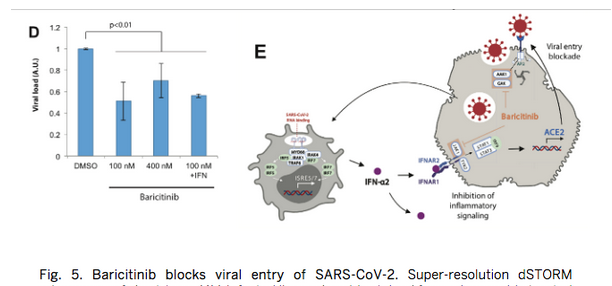
En el campo terapéutico, sin embargo, no hay mayores variantes, si bien caen las tasas de mortalidad del Covid-19, ante una atención mejorada de las salas de cuidados intensivos y la administración de medicamentos como la dexametasona, remdesivir, anticuerpos monoclonales, y el mejor entrenamiento y equipamiento de los trabajadores de la salud. Los agentes terapéuticos, sin embargo, siguen aún en disputa, como el remdesivir, al igual que anticuerpos monoclonales como el de Lilly si bien uno de ellos resultó aprobado por la FDA. Otro anticuerpo que corrió con peor suerte es aquél dirigido contra la interleucina 6, lo cual sugiere que ese no es el bloqueo terapéutico más adecuado. Para complicar aún más el tratamiento antivirual, el SARS-CoV-2 nos revela otros trucos que aumentan su poder de transmisión aparte de las mutaciones, y es el uso de la maquinaria celular como accesorio para la invasión, como lo demuestra el reciente descubrimiento del rol de los ácidos grasos en el movimiento de las bisagras de la espiga, y ahora el virus nos sale con la ayuda de las neuropilinas que favorecen la invasión celular, y ni hablar del rol de la proteína quinasa Jano, JAK, en la fisiopatología hepática, solo que la inhibición de JAK reduce la infectividad hepática del SARS-CoV-2 y modula las respuestas inflamatorias para reducir la morbilidad y la mortalidad.
La contención y mitigación apunta ahora hacia dos frentes principales, el entorno familiar que sigue siendo muy importante para la transmisión de la pandemia; y el uso de mascarillas para evitar la Infección por SARS-CoV-2 adquirida en el hospital. Los hallazgos sobre infecciones nosocomiales de Covid-19 sugieren que la transmisión hospitalaria general del SARS-CoV-2 en el contexto de la protección con mascarillas de trabajadores de la salud y pacientes es escasa, incluso durante los períodos de alta prevalencia en la comunidad. Esto tiene al menos 2 implicaciones importantes. En primer lugar, es imperativo que el público comprenda que los hospitales con políticas de protección universal con mascarillas, bien implementadas, son abrumadoramente seguros; y en segundo lugar, que los mensajes de salud pública deben enfatizar que no es necesario evitar o retrasar la atención médica necesaria y urgente.
Lo más visto en la semana
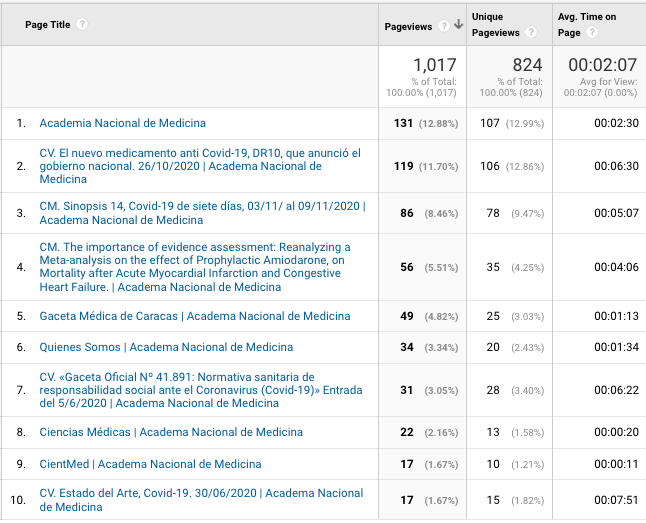
La Semana en Resumen
Vacunas
MODERNA. Lunes 16/11/2020. Moderna, Inc. anunció hoy que el Data Safety Monitoring un comité independiente designado por los NIH y la Junta (DSMB) para el estudio de fase 3 de mRNA-1273 sobre la vacuna candidata contra COVID-19, informó a Moderna que el ensayo cumplió con los criterios estadísticos pre-especificados en el protocolo del estudio para la eficacia, con una eficacia de la vacuna del 94,5%. Este estudio, conocido como el estudio COVE, inscribió a más de 30,000 participantes en los EE. UU. y se está realizando en colaboración con el Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAID), parte de los Institutos Nacionales de Salud (NIH) y el Instituto Biomédico. Autoridad de Investigación y Desarrollo Avanzado (BARDA), parte de la Oficina del Subsecretario de Preparación y Respuesta del Departamento de Salud y Servicios Humanos de EE. UU. El criterio de valoración principal del estudio de fase 3 COVE, se basa en el análisis de los casos de COVID-19 confirmados y adjudicado a partir de dos semanas después de la segunda dosis de vacuna. Este primer análisis intermedio se basó en 95 casos, de los cuales se observaron 90 casos de COVID-19 en el grupo de placebo versus 5 casos observados en el grupo de ARNm-1273, lo que resultó en una estimación puntual de la eficacia de la vacuna del 94,5% (p <0,0001).
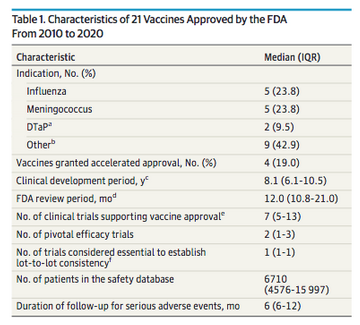
JAMA INTERNAL MEDICINE, Martes 10/11/2020. Velocidad, evidencia y características de seguridad de las aprobaciones de vacunas por la Administración de Alimentos y Medicamentos de EE. UU, FDA. Desde 2010, la mayoría de las vacunas novedosas aprobadas por la FDA requirieron alrededor de 8 años de desarrollo clínico y se basaron en la evidencia de una mediana de 7 ensayos clínicos, incluidos al menos 2 ensayos fundamentales de eficacia que fueron aleatorizados, enmascarados y que utilizaron un grupo comparador . Estos ensayos fundamentales de eficacia incluyeron una mediana de 5000 pacientes, que fueron seguidos para eventos adversos graves durante al menos 6 meses. Dada la urgencia de desarrollar una vacuna COVID-19, los ensayos deberán ser más grandes que los que respaldan las aprobaciones previas de la vacuna e incluir suficiente tiempo de seguimiento para la aparición de efectos adversos.
NATURE. Martes 10/11/2020. ¿Qué significan los resultados de la vacuna COVID de Pfizer para la pandemia? Un comentario de Nature reune la opinión de varios expertos sobre importantes asuntos pendientes de la vacuna de Pfizer: Lo que falta, dicen Eric Topol y otros científicos, son detalles sobre la naturaleza de las infecciones contra las que la vacuna puede proteger, ya sean en su mayoría casos leves de COVID-19 o también incluyen un número significativo de casos moderados y graves. «Quiero saber el espectro de enfermedades que previene la vacuna», dice Paul Offit, científico de vacunas del Children’s Hospital of Philadelphia en Pensilvania, que forma parte de un comité asesor de la Administración de Alimentos y Medicamentos de EE. UU. No está claro si la vacuna puede evitar que las personas que no muestran síntomas de COVID-19 o que solo muestran síntomas muy leves propaguen el coronavirus. Una vacuna que bloquee la transmisión podría acelerar el fin de la pandemia. Una pregunta clave sin respuesta es ¿cuánto durará la eficacia de la vacuna? Expresa, Rafi Ahmed, inmunólogo de la Universidad Emory en Atlanta. Georgia: “Para mí, la pregunta principal es qué pasa seis meses después, o incluso tres meses después”.
SCIENCE, Viernes 13/11/2020. La eficacia de la vacuna en grupos de alto riesgo y la reducción de la diseminación viral son importantes para la protección. Es probable que las preguntas sobre las características de la vacuna COVID-19 queden sin respuesta, incluso después de que se completen los ensayos. En primer lugar, los ensayos no suelen tener el poder estadístico suficiente para establecer la eficacia específica de subgrupos, pero el rendimiento de la vacuna en grupos de alto riesgo afecta el éxito de una estrategia de protección directa. En segundo lugar, ¿pueden las vacunas prevenir la infección o reducir el contagio? Esto es importante para lograr una protección directa. Ampliar los esfuerzos en curso o planificar nuevos estudios puede generar los datos necesarios para abordar estas preguntas…
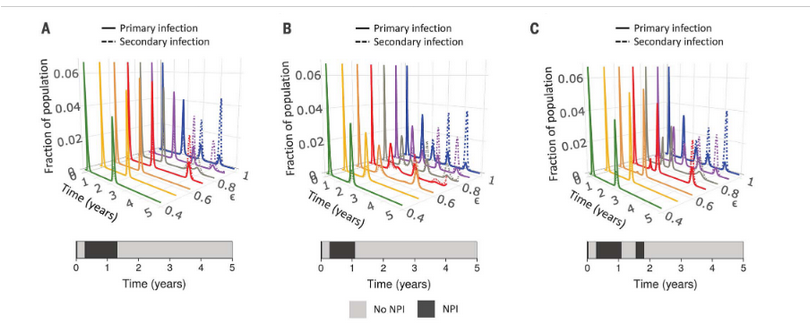
SCIENCE. Viernes 13/11/2020. Historia de vida inmunitaria, vacunación y dinámica del SARS-CoV-2 durante los próximos 5 años. La trayectoria futura de la pandemia de la enfermedad por coronavirus 2019 (COVID-19) depende de la dinámica de la inmunidad adaptativa contra el síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2); sin embargo, las características sobresalientes de la respuesta inmune provocada por la infección natural o la vacunación aún son inciertas. Utilizamos modelos epidemiológicos simples para explorar estimaciones de la magnitud y el momento de los casos futuros de COVID-19, dando diferentes supuestos con respecto a la eficacia protectora y la duración de la respuesta inmune adaptativa al SARS-CoV-2, así como su interacción con vacunas e intervenciones no farmacéuticas. Descubrimos que las variaciones en la respuesta inmune a las infecciones primarias por SARS-CoV-2 y una posible vacuna pueden generar paisajes inmunes muy diferentes y cargas de casos críticamente graves, que van desde epidemias sostenidas hasta casi la eliminación.
SCIENCE. Sábado 14/11/2020. Fuertes críticas a la vacuna rusa Gamaleya. Un mes antes del lanzamiento del ensayo de eficacia del Sputnik V en septiembre, la vacuna Gamaleya recibió una aprobación muy controvertida de las autoridades reguladoras rusas, que permitió que se administrara a personas fuera de un ensayo clínico. El comunicado de Gamaleya dice que la vacuna se ha utilizado en las «zonas rojas» de los hospitales rusos, lo que significa trabajadores de la salud y otros grupos de alto riesgo. Hasta la fecha, el comunicado dice que 10,000 personas han recibido la vacuna bajo esta autorización. «[El uso civil de la vacuna fuera de los ensayos clínicos también confirmó la tasa de eficacia de la vacuna de más del 90 por ciento», dice el comunicado de Gamaleya sin ofrecer ninguna evidencia que respalde esta afirmación. Pfizer y BioNTech y muchas otras empresas han hecho públicos sus protocolos de prueba, pero Gamaleya no. Zavidova señala que aprendió más sobre los detalles del estudio de Gamaleya en un sitio web de ensayos clínicos mantenido por los NIH que en un registro similar en Rusia, que tiene «solo el nombre de este protocolo sin ningún detalle».
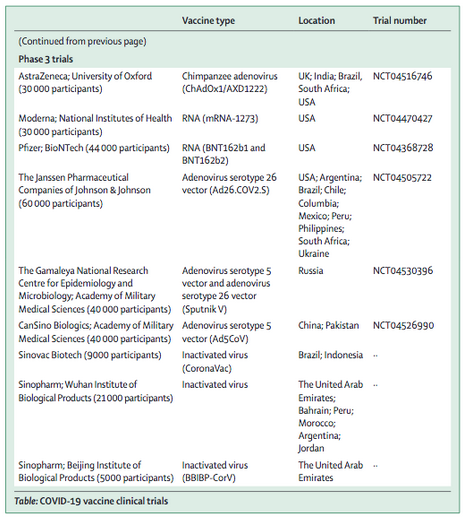
THE LANCET. Sábado 14/11/2020. Inmunidad al SARS-CoV-2: revisión y aplicaciones a vacunas candidatas de fase 3. Esta revisión analiza lo que se sabe actualmente sobre las respuestas inmunitarias humorales y celulares humanas al coronavirus 2 del síndrome respiratorio agudo severo y relacionamos este conocimiento con las vacunas COVID-19 que se encuentran actualmente en ensayos clínicos de fase 3. Queda mucho por aprender con respecto a la inmunidad al coronavirus en general y la inmunidad al SARS-CoV-2 en particular, incluida la inmunidad protectora inducida por las vacunas y el mantenimiento de la inmunidad contra este virus. Además, probablemente se necesitarán múltiples tipos de vacunas en diferentes poblaciones (p. Ej., Lactantes inmaduros inmunes, niños, mujeres embarazadas, individuos inmunodeprimidos e individuos inmunosenescentes de 65 años o más). Además de la respuesta inmune adaptativa, hay algunos datos que sugieren que la inmunidad innata entrenada también podría tener un papel en la protección contra COVID-19. Múltiples ensayos clínicos (p. Ej., NCT04327206, NCT04328441, NCT04414267 y NCT04417335) están examinando si vacunas no relacionadas , como la vacuna contra el sarampión, las paperas y la rubéola y la vacuna contra el Bacillus Calmette-Guérin, pueden provocar una inmunidad innata entrenada y conferir protección contra COVID-19.
Tratamiento
FDA. Martes 10/11/2020. Actualización del coronavirus (COVID-19): Autorización del anticuerpo monoclonal de Lilly para el tratamiento del COVID-19. La Administración de Drogas y Alimentos de EE. UU., emitió una autorización de uso de emergencia (EUA) para la terapia con anticuerpos monoclonales en investigación bamlanivimab para el tratamiento de COVID-19 leve a moderado en pacientes adultos y pediátricos. Bamlanivimab está autorizado para pacientes con resultados positivos de pruebas virales directas del SARS-CoV-2 que tengan 12 años de edad o más y pesen al menos 40 kilogramos (aproximadamente 88 libras) y que tengan un alto riesgo de progresar a COVID-19 y / u hospitalización. Esto incluye a aquellos que tienen 65 años de edad o más, o que tienen ciertas afecciones médicas crónicas.
NATURE. Miércoles 11/11/2020. ¿Por qué parecen estar cayendo las tasas de mortalidad por COVID? Hasta ahora, los esteroides son el único medicamento que ha demostrado tener un efecto dramático sobre la mortalidad por COVID-19. «Cualquiera que esté muy enfermo debería recibir esteroides», dice Angus. «Y todo lo demás es un juego de azar». También se están realizando pruebas de anticuerpos purificados, como las que evalúan la mezcla de dos anticuerpos producidos por la empresa de biotecnología Regeneron Pharmaceuticals en Tarrytown, Nueva York, que se administró al presidente de Estados Unidos, Donald Trump. Estos se dirigen principalmente a personas que tienen síntomas leves de COVID-19. A pesar de las afirmaciones de Trump de que el tratamiento fue una «cura», aún no se han completado grandes ensayos del cóctel y no hay evidencia de que tenga un impacto en las tasas de muerte por COVID-19. Un estudio de los Institutos Nacionales de Salud de EE. UU. Ha demostrado que el medicamento antiviral remdesivir, desarrollado por la empresa biofarmacéutica Gilead Sciences en Foster City, California, acorta las estadías en el hospital. Un ensayo posterior coordinado por la Organización Mundial de la Salud descubrió que el medicamento tenía poco efecto, si es que tenía alguno, sobre la mortalidad, pero la Administración de Alimentos y Medicamentos de EE. UU. lo aprobó para el tratamiento de COVID-19 el 22 de octubre. Suprimir la transmisión es la mejor manera de reducir las muertes por COVID-19: ‘Asegurémonos de que las personas de 70 y 80 años no ‘no se infecten».
THE LANCET. Miércoles 11/11/2020. Aprovechando la respuesta del COVID-19 para poner fin a las muertes infantiles evitables por neumonía. Aunque la mayoría de los niños tienen menos enfermedades relacionadas con COVID-19 que los adultos, los posibles impactos secundarios de la pandemia podrían provocar una reversión en el progreso de la supervivencia infantil. Roberton y sus colegas utilizaron un modelo para estimar que, según el grado de gravedad, las interrupciones del servicio, las reducciones en el acceso a la atención debido a las medidas de bloqueo y el aumento de las tasas de desgaste debido a la escasez de alimentos durante 12 meses podrían causar entre 506900 y 2313900 muertes adicionales entre niños menores de 5 años. Los datos sugieren que alrededor de un tercio de estas muertes evitables podrían deberse a neumonía y sepsis neonatal.
Seis acciones estratégicas para acabar con las muertes por neumonía
1 Desarrollar e implementar estrategias de control de la neumonía
2 Dar prioridad a las poblaciones vulnerables
3 Financiar adecuadamente el control y el tratamiento de la neumonía.
4 Acelerar las innovaciones revolucionarias .Aumentar la inversión en investigación y desarrollo en áreas donde las tecnologías y sistemas rentables aumentan la eficiencia y previenen la mayoría de las muertes por neumonía.
5 Realice un seguimiento del progreso con transparencia, responsabilidad e inclusión.
6 Fortalecer las alianzas. Involucrar a todos los actores sanitarios y no sanitarios, privados y públicos a nivel mundial y nacional.
PREPRINT. Jueves 12/11/2020. Documento de trabajo sobre las mutaciones en pico del SARS-CoV-2 que surgen en el visón danés, su propagación a los humanos y los datos de neutralización. Las mutaciones de la espiga del virus dentro del visón infectado dieron lugar a varios cambios de aminoácidos en la proteína de pico. La primera fue una tirosina a fenilalanina en el aminoácido 453 (Y453F), una mutación que también apareció durante los brotes de granjas de visones holandeses. Es una sustitución conservadora de aminoácidos en el dominio de unión al receptor que contacta directamente con el receptor ACE2 del huésped en el aminoácido 34 (Wang et al.). Esta posición de contacto de ACE2 difiere entre humanos y visones (histidina [34H] en seres humanos y tirosina [34Y] en visones y otros mustélidos (Damas et al.)), lo que sugiere que Y453F es una mutación de adaptación al ACE2 de visón. Es importante destacar que 453F aumenta la afinidad por ACE2 humano , que puede explicar su exitosa introducción y establecimiento en humanos.
SCIENCE ADVANCES. Viernes 13/11/2020. La inhibición de JAK [proteína quinasa jano] reduce la infectividad hepática del SARS-CoV-2 y modula las respuestas inflamatorias para reducir la morbilidad y la mortalidad. Mediante el uso de inteligencia artificial, IA, identificamos que el baricitinib posee eficacia antiviral y anticitocina. Ahora mostramos un beneficio de mortalidad del 71% (IC del 95%: 0,15-0,58) en 83 pacientes con neumonía por SARS-CoV-2 de moderada a grave con pocos eventos adversos inducidos por fármacos, incluida una gran cohorte de ancianos (mediana de edad 81 años). Otros 48 casos de neumonía leve a moderada se recuperaron sin problemas. Usando cultivos organotípicos en 3D de células primarias de hígado humano, demostramos que el interferón-alfa-2 (IFNα2) aumenta significativamente la expresión de ACE2 y la infectividad del SARS-CoV-2 en células parenquimatosas en> 5 veces.
SCIENCE. Viernes 13/11/2020. Facilitación de la infección de la célula huésped por SARS-CoV-2. Los resultados sugieren la interacción proteína S-NRP1 como un objetivo antiviral potencial. En las páginas 861 y 856 de este número de Science, Daly et al. (1) y Cantuti-Castelvetri et al. (2), respectivamente, muestran que la proteína de membrana neuropilina-1 (NRP1) promueve la entrada del SARS-CoV-2 y explican cómo NRP1 interactúa con la proteína SARS-CoV-2 S. La neuropilina-1 se une a la proteína espiga procesada con furina de SARS-CoV-2 para promover la entrada del virus. Las neuropilinas son una familia de proteínas de membrana que se identificaron originalmente debido a su participación en la angiogénesis (formación de vasos sanguíneos) y la guía axilar. Las neuropilinas también son correceptores de moléculas como los factores de crecimiento endotelial vascular (VEGF) y las semaforinas, y estudios recientes han demostrado su hiperregulación durante la angiogénesis tumoral y su potencial como dianas contra el cáncer.
NEJM. Sábado 14/11/2020. Una serie de resultados decepcionantes de variados ensayos clínicos sobre las terapias inmunitarias para COVID-19. En unas notables 48 horas a fines del mes pasado (del 21 al 23 de octubre, para ser exactos), aparecieron impresos no menos de cuatro ensayos clínicos aleatorios multicéntricos de tocilizumab (contra Interleucina 6): tres en revistas revisadas por pares y uno como preimpresión. Todos se realizaron en pacientes hospitalizados que no recibieron ventilación mecánica, y todos compararon tocilizumab con un control de “atención habitual”. Ver:
RCT-TCZ-COVID-19 (n = 126): el criterio principal de valoración fue hipoxemia (definido por el protocolo), ingreso en la UCI o muerte. Los investigadores detuvieron el estudio antes de tiempo debido a su inutilidad.
CORIMUNO-19-TOCI-1 (n = 131): dos criterios de valoración fueron de interés principal: puntuaciones superiores a 5 en la escala de progresión clínica de 10 puntos de la OMS (WHO-CPS) en el día 4 y supervivencia sin necesidad de ventilación (incluida ventilación no invasiva) en el día 14. Tocilizumab no demostró eficacia en la primera medida y «podría» (cito el artículo) haber reducido la necesidad de ventilación mecánica (los resultados fueron dudosos). Sin impacto en la mortalidad.
Ensayo BACC Bay Tocilizumab (n = 243): a diferencia de los dos primeros, este fue un ensayo controlado con placebo, con una aleatorización 2: 1 a tocilizumab o placebo. Tocilizumab no redujo significativamente la necesidad de intubación o la mortalidad, el criterio de valoración principal. Dado que los intervalos de confianza alrededor de la estimación puntual para el beneficio o el daño fueron amplios, el estudio no pudo excluir ninguno de los dos.
EMPACTA (n = 389): también controlado con placebo, el criterio de valoración principal de este estudio fue la muerte o la ventilación mecánica el día 28. Aquí, tocilizumab redujo el riesgo de ventilación mecánica, pero la mortalidad al día 28 no mejoró; curiosamente, fue numéricamente mayor con el tratamiento (10,4% vs 8,6%). (El estudio aún no ha sido revisado por pares).
Diagnóstico
SCIENCE. Jueves 12/11/2020. La variante de SARS-CoV-2, D614G, exhibe una replicación eficiente ex vivo y transmisión in vivo. La sustitución D614G de la espiga del virus prevalece en las cepas globales de SARS-CoV-2, pero sus efectos sobre la patogénesis viral y la transmisibilidad siguen sin estar claros. Diseñamos una variante de SARS-CoV-2 que contiene esta sustitución. La variante exhibe infección, replicación y aptitud competitiva más eficientes en las células epiteliales primarias de las vías respiratorias humanas, pero mantiene una morfología y propiedades de neutralización in vitro similares, en comparación con el virus ancestral de tipo silvestre.
NATURE. Viernes 13/11/2020. El análisis del visón COVID muestra que las mutaciones no son peligrosas, todavía. Los científicos que han revisado los datos sobre la propagación del SARS-CoV-2 a visones, dicen que las mutaciones en sí mismas no son particularmente preocupantes porque hay poca evidencia de que permitan que el virus se propague más fácilmente entre las personas, lo haga más letal o ponga en peligro la terapéutica y las vacunas. “Las mutaciones asociadas al visón que conocemos no están asociadas con una propagación rápida, ni con cambios en la morbilidad y la mortalidad”, dice Astrid Iversen, viróloga de la Universidad de Oxford, Reino Unido.
JAMA. Viernes 13/11/2020. La necesidad de realizar más y mejores pruebas para COVID-19. Las pruebas que pueden identificar rápidamente a muchas personas con virus infecciosos (en lugar de simplemente ARN viral), incluso cuando las personas no presentan síntomas, podrían limitar la propagación de la infección y ayudar a prevenir brotes grandes. Las pruebas de antígenos tienen el potencial de cumplir este papel. Estas pruebas capturan proteínas virales en un formato de flujo lateral rápido que puede ser realizado fácilmente por personal no capacitado y dan resultados en menos de 15 minutos. Aunque son menos sensibles que las pruebas de reacción en cadena de la polimerasa con transcriptasa inversa, los primeros datos sugieren que las pruebas de antígenos se pueden utilizar para diagnosticar a las personas con virus infecciosos durante la infección sintomática por COVID-19. Las pruebas de antígenos pueden desempeñar un papel clave en la identificación rápida de las personas con mayor riesgo para transmitir enfermedades. Sin embargo, el rendimiento de las pruebas en personas sin síntomas no se comprende bien y se necesita urgentemente más investigación sobre el valor de estas pruebas.
TABLERO JOHNS HOPKINS. Lunes 16/11/2020. Venezuela en plena fase exponencial de la pandemia supera los 97.000 (97.352) casos confirmados, acumula 851 fallecidos, y dibuja una aparente e irregular caida del pico de casos en noviembre 2020.
Contención y Mitigación
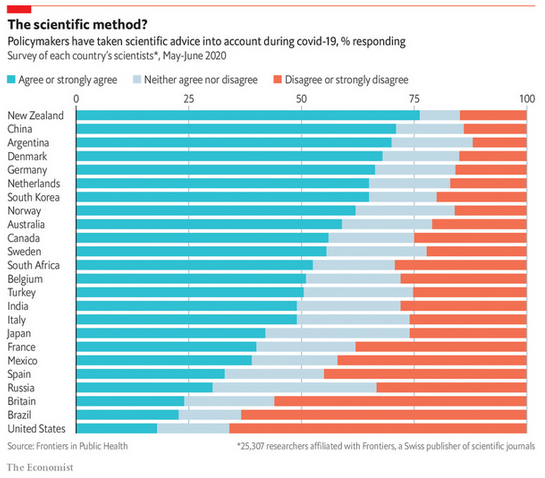
THE ECONOMIST. Miércoles 11/11/2020. ¿Están los gobiernos siguiendo la ciencia sobre el Covid-19? AX WEBER, un sociólogo alemán, sostuvo que la política y la ciencia no se mezclan. Hoy, con la pandemia del Covid-19 en todo el mundo, los gobiernos no tienen más remedio que entrar en este matrimonio infeliz. Una encuesta realizada por Frontiers, una editorial suiza de revistas científicas, preguntó a unos 25.000 investigadores en mayo y junio si los legisladores de su país habían utilizado el asesoramiento científico para informar su estrategia Covid-19. Los resultados ofrecen cierto apoyo a la tesis de Weber. Según la encuesta, los investigadores de Nueva Zelanda están más satisfechos con los formuladores de políticas. Más de las tres cuartas partes de los encuestados coincidieron en que el gobierno de Jacinda Ardern, que cerró las fronteras del país e impuso un estricto bloqueo a principios de marzo, ha tenido en cuenta el asesoramiento científico de expertos. No es de extrañar, ya que Nueva Zelanda ha eliminado el virus dos veces. La respuesta de la Sra. Ardern también ha sido popular entre los votantes. El 17 de octubre obtuvo una abrumadora victoria en las elecciones generales del país.
JAMA. Viernes 13/11/2020. Infección por SARS-CoV-2 adquirida en el hospital Lecciones de salud pública. Los hallazgos sobre infecciones nosocomiales de Covi-19 sugieren que la transmisión hospitalaria general del SARS-CoV-2 en el contexto de la protección con mascarillas de trabajadores de la salud y pacientes es escasa, incluso durante los períodos de alta prevalencia en la comunidad. Esto tiene al menos 2 implicaciones importantes. En primer lugar, es imperativo que el público comprenda que los hospitales con políticas de protección universal con mascarillas, bien implementadas, son abrumadoramente seguros, y los mensajes de salud pública deben enfatizar que no es necesario evitar o retrasar la atención médica necesaria y urgente. En segundo lugar, a pesar de la politización del enmascaramiento, esta es una prueba de concepto importante y convincente para el uso más amplio del enmascaramiento universal en ambientes interiores abarrotados, incluso con buena ventilación.











Mi preguntas son si la «vacuna» actúa en ARN mensajero ¿Que consecuencias a futuro tendrá en mi ADN?
¿En cuántas generaciones de animales de laboratorio se hicieron estudios?
¿Cómo será el ADN de la próxima generación de Humanos?
¿Es una vacuna o una manipulación genetica?
¿Por que no hicieron ese anuncio en octubre si ya tenían los resultados?
Gracias por su comentario e interés en nuestra página. Con relación a sus preguntas: 1) La relación de la vacuna con el ADN, no creo que haya ninguna, pues la única forma de tener alguna influencia sobre el genoma humano, del ARNm de la espiga del virus, es mediante una transcriptasa en reverso que lo transforme en ADN y de allí que pueda luego insertar esa secuencia en el genoma del huésped, medìante un proceso desconocido y altamente improbable sino imposible. 2) La empresa Moderna o Pfizer no dio detalles técnicos sobre las pruebas en animales (preclínicas), tenga presente usted que los reportados son ensayos clínicos de la fase 3. Esperemos los artículos respectivos en revistas arbitradas e indizadas. 3) El ADN de la «proxima generación de humanos» podría seguir este patrón evolutivo publicado en Nature Genetics en 2011: « Los cambios evolutivos en humanos se desarrollan con bastante frecuencia, pero no se «pegan»: pues se necesita alrededor de un millón de años para que un rasgo evolutivo se desarrolle y dure.. 4) Las dos vacunas, Moderna y Pfizer, son de ARNm, las otras tres que vienen, AstraZeneca, Lilly y J&J, en fase 3, usan adenovirus modificados por ingeniería genética. 5) Pregunte a Pfizer y Moderna ¿por qué no hicieron el anuncio antes?, si bien dudo mucho que para ese entonces, octubre, ambas empresas conocieran de antemano lo que un comité independiente formado por científicos del más alto nivel, le iban a reportar en noviembre. Le recuerdo, por si no lo sabe, que las empresas reportan lo que les dice una comisión científica designada por los Institutos de Salud de los Estados Unidos, el NIH. Lea bien, por favor, lo que dice la Sinopsis 15 y sus hipertextos, que lo llevan del nivel poblacional al celular y molecular.